Peste dei piccoli ruminanti in Europa: l’allarme 2024–2025 e la nuova frontiera della sorveglianza
Introduzione
La peste dei piccoli ruminanti (PPR) è una malattia virale altamente contagiosa che colpisce principalmente pecore e capre, sebbene possa coinvolgere anche altri ruminanti domestici e selvatici. È causata da un virus appartenente al genere Morbillivirus (famiglia Paramyxoviridae), filogeneticmanete correlato al virus della peste bovina, e di cui sono stati identificati 4 lignaggi genetici (I-IV)1. La malattia si manifesta con un quadro clinico che può includere febbre, abbattimento, lesioni del cavo orale, scolo oculonasale, sintomatologia respiratoria e diarrea, con tassi di mortalità generalmente compresi tra il 20% e il 90%, fino a raggiungere valori prossimi al 100% nelle popolazioni suscettibili2.
Con perdite stimate dalla Food and Agricolture Organization of the United Nations (FAO) tra 1,3 e 2 miliardi di euro all’anno3, l’eradicazione della PPR entro il 2030 rappresenta un obiettivo condiviso dalla comunità internazionale e si inserisce nell’iniziativa congiunta FAO-World Animal Health Organization (WOAH) per l’eradicazione globale della PPR, basata sull’integrazione tra vaccinazione, diagnostica e rafforzamento dei servizi veterinari.
La PPR si trasmette principalmente per contatto diretto tra animali infetti, attraverso secrezioni ed escrezioni, in particolare quelle respiratorie; la trasmissione indiretta attraverso fomiti è possibile, ma riveste un ruolo secondario. Il periodo di incubazione è in media di 5 - 6 giorni, durante il quale il virus può già essere eliminato e trasmesso ad altri animali1.
Dal punto di vista epidemiologico, un ruolo determinante nella diffusione della PPR è svolto dalla movimentazione degli animali, in particolare in contesti di commercio informale e transfrontaliero, che può consentire l’introduzione silente del virus in nuove aree e in popolazioni suscettibili. In tali condizioni, la malattia può diffondersi rapidamente, determinando focolai caratterizzati da elevata morbilità e mortalità.
La diagnosi si basa sulla valutazione clinico-epidemiologica seguita dalla conferma di laboratorio. Questa può essere eseguita con RT-PCR, considerato il gold standard per la conferma diagnostica, test sierologici (ELISA), e isolamento e sequenziamento virale. I campioni idonei includono tamponi nasali, oculari e rettali, sangue intero in EDTA, siero, organi (linfonodi, polmone, milza) e carcasse intere1.
Nel quadro normativo europeo, la PPR è classificata come malattia di Categoria A, ovvero una malattia che non dovrebbe essere presente sul territorio dell’Unione Europea (UE) e per la quale, alla conferma, si applicano misure finalizzate all’eradicazione immediata. Queste includono l’abbattimento obbligatorio di tutti gli animali recettivi detenuti nell’allevamento infetto, seguito dallo smaltimento sicuro delle carcasse come materiale di categoria 1 ai sensi dell’articolo 8 del Regolamento (CE) n. 1069/20094. Contestualmente, attorno al focolaio vengono istituite zone di restrizione obbligatorie: una zona di protezione con un raggio minimo di 3 km e una zona di sorveglianza con un raggio minimo di 10 km, in cui si applicano severe limitazioni alle movimentazioni di animali e prodotti. All'interno di queste zone vengono imposte restrizioni alla movimentazione e viene condotto un intenso screening tramite controlli clinici e indagini di laboratorio sugli allevamenti.
Le disposizioni operative relative alla gestione del sospetto e della conferma, all’istituzione delle zone soggette a restrizione e alle misure applicabili agli stabilimenti interessati si collocano nel quadro dell’Animal Health Law e dei relativi atti delegati e di esecuzione.
In particolare, il Regolamento (UE) 2016/4295 costituisce il quadro normativo generale, mentre il Regolamento delegato (UE) 2020/6876 definisce le misure di prevenzione e controllo per le malattie di categoria A, inclusa la PPR.
Sebbene non si tratti di una zoonosi, la malattia ha rilevanza sanitaria ed economica, determinando conseguenze economiche significative legate alla riduzione delle produzioni, l’incremento delle perdite dirette e indirette, e alle restrizioni alle movimentazioni e agli scambi adottate per contenere la diffusione del virus.
Tradizionalmente considerata una minaccia prevalente per ampie aree di Africa, Medio Oriente e Asia, con una sempre maggiore prevalenza del lignaggio IV7, la comparsa di primi focolai in Bulgaria nel 2018 e le successive incursioni in Grecia e Romania nel 2024 hanno evidenziato la vulnerabilità dell’Unione Europea (UE) e un concreto rischio di introduzione in altri Paesi dell’area, imponendo una revisione urgente delle strategie di prevenzione, controllo ed eradicazione.
In questo articolo analizziamo la sequenza di incursioni che ha progressivamente spostato il fronte epidemiologico, le nuove conoscenze che guidano la risposta sanitaria e l'evoluzione dei sistemi di sorveglianza fondamentali per proteggere Paesi ancora indenni come l'Italia.
Situazione epidemiologica in Europa: sviluppi dal 2024
La peste dei piccoli ruminanti è stata descritta per la prima volta nel 1942 in Costa d’Avorio e, per quanto riguarda il continente europeo, una prima conferma risale al 2000 nella regione della Tracia orientale, la porzione europea della Turchia1.
La percezione dell'Europa come continente sostanzialmente indenne dalla PPR è stata profondamente ridimensionata nel biennio 2024-2025. Se eventi precedenti, come il focolaio registrato in Bulgaria nel 2018, potevano essere interpretati come incursioni sporadiche e circoscritte, gli sviluppi più recenti delineano uno scenario epidemiologico mutato: la PPR ha stabilito una presenza attiva nel Sud-Est europeo, con il rischio di ulteriore consolidamento ed espansione geografica. In particolare, nel luglio 2024 la malattia è stata notificata per la prima volta in Grecia e pochi giorni dopo in Romania; a questi eventi sono seguite, nel corso del 2024 e 2025, ulteriori notifiche di focolai in Bulgaria, Ungheria, Albania e Croazia, Paesi dell’UE, o immediatamente limitrofi, che in precedenza risultavano indenni.
2024–2025: cronologia delle incursioni nel Sud-Est Europa8,9
Grecia (2024)10,11: a luglio viene confermato il primo focolaio di PPR in Tessaglia, nella Grecia centro-settentrionale nelle prefetture di Trikala e Larisa. Successivamente vengono notificati decine di focolai distribuiti in altre regioni del Paese. La Tessaglia ospita circa 1,7 milioni di piccoli ruminanti distribuiti in 8.500 allevamenti, con oltre 1 milione di capi concentrati solo nella prefettura di Larisa. Questa elevata densità e la pratica diffusa del pascolo promiscuo hanno favorito la rapida diffusione del virus. Il ritardo nella diagnosi del primo focolaio, inizialmente scambiato per febbre catarrale degli ovini (Bluetongue), ha permesso al virus di diffondersi prima dell’introduzione delle misure di restrizioni sanitarie. Nonostante l’adozione successiva di misure di controllo, quali l’implemetazione di zone di restrizione, la disinfezione, il controllo dei movimenti e la sorveglianza sul territorio, la malattia continua a diffondersi. A novembre 2024, quando si ritiene l'emergenza ormai conclusa, la Grecia notifica nuovi focolai nelle unità regionali di Corinzia ed Elide, nel sud del Paese. Le indagini epidemiologiche hanno identificato diversi fattori critici nella diffusione dell’epidemia, tra cui l’intenso commercio di animali, le carenze di biosicurezza (in particolare nei camion per la raccolta del latte) e i movimenti di animali avvenuti prima dell’introduzione delle restrizioni, quando alcuni soggetti erano già in fase di incubazione.
Romania (2024)12,13: i primi focolai di PPR vengono notificati a luglio 2024 nelle contee di Tulcea e Costanza, nella parte sud-orientale del Paese. In questo caso la dimensione degli allevamenti colpiti risulta particolarmente rilevante: tra gli stabilimenti infetti, uno supera i 50,000 ovini, altri 2 contano rispettivamente 12,000 e 19,000 capi. Nel giro di pochi giorni il virus si diffonde per 500 chilometri e raggiunge la contea di Timiș, nell’estremità occidentale del Paese. Ad agosto 2024 un nuovo focolaio viene confermato nella contea di Lalomița, a 80 chilometri a sud-ovest dal primo cluster in Tulcea. La Commissione Europea, modificando per la seconda volta le zone soggette a restrizione, segnala un rischio molto elevato di ulteriore diffusione dell’infezione. In seguito alla chiusura di questo primo evento epidemico, viene notificato a marzo 2025 un nuovo evento associato alla comparsa di focolai nella regione di Crișana, a nord-ovest.
Bulgaria (2024): a fine novembre la Bulgaria notifica ufficialmente un focolaio di PPR nella regione di Pazardzhik, nel sud del Paese, sebbene i primi sintomi fossero stati osservati diverse settimane prima. L’infezione coinvolge 5 allevamenti appartenenti alla stessa famiglia, con animali allevati in modo estensivo e pascolo promiscuo. Gli allevatori presentano ricorso al tribunale contro le misure di abbattimento, ottenendone la sospensione; tuttavia, un secondo campionamento conferma la positività degli animali. L’evento genera una forte reazione negativa da parte dell’opinione pubblica, complicando ulteriormente l’attuazione delle misure sanitarie. I controlli clinici e di laboratorio effettuati su oltre 8.000 animali nelle aree epidemiologicamente collegate, non rilevano ulteriori focolai. Le autorità bulgare istituiscono pertanto zone di protezione (5 km) e di sorveglianza (20 km). Nonostante le misure adottate, il focolaio risulta ancora attivo e il rischio di ulteriore diffusione dell’infezione nella regione rimane elevato.
Ungheria (2025)14,15: a gennaio 2025 un focolaio di PPR viene confermato nella provincia di Zala, situata nell'estremità sud-occidentale dell'Ungheria, a soli 3 chilometri dal confine con la Slovenia. L'indagine epidemiologica riconduce verosimilmente l'introduzione del virus a un lotto di agnelle importate dalla Romania, Paese già interessato da numerosi focolai. Le analisi filogenetiche collocano il ceppo ungherese nel lineage IV, strettamente correlato ai ceppi circolanti in Romania, Grecia e Bulgaria. A seguito della notifica vengono prontamente messe in atto le misure di contenimento previste. Successivamente si registrano 2 focolai secondari epidemiologicamente collegati al focolaio primario: uno attribuito a contatto diretto tra gli animali e l’altro associato all’acquistato di fieno proveniente da un allevamento coinvolto nel focolaio primario. Tutti gli allevamenti infetti vengono sottoposti ad abbattimento totale e disinfezione; le operazioni si concludono a febbraio, consentendo la chiusura del focolaio. A titolo precauzionale la Slovenia istituisce una propria zona di sorveglianza lungo il confine. Questo episodio evidenzia il potenziale ruolo delle importazioni di animali vivi dai Paesi balcanici nell’introduzione del virus in aree precedentemente indenni.
Albania (2025): a giugno 2025 vengono notificati i primi focolai, con infezioni che compaiono pressoché simultaneamente in diverse aree del Paese: dal distretto di Scutari (nord-ovest), ai distretti montuosi di Dibër e Bulqizë (nord-est), fino alle aree interne di Skrapar (centro-sud) e quelle di Polenë e Devoll (sud-est), al confine con la Grecia. I focolai interessano esclusivamente i capi caprini; ciò ha portato a ipotizzare una possibile circolazione subclinica negli ovini oppure una diversa suscettibilità tra le 2 specie. L'indagine epidemiologica non identifica con certezza la fonte di introduzione; tuttavia, si sospetta che il virus sia entrato nel Paese attraverso movimenti illegali di animali o tramite l’importazione di agnelli potenzialmente infetti. La concomitanza con la festività del Kurban Bayram (6 giugno), periodo caratterizzato da un aumento di scambi e della movimentazione di piccoli ruminanti, potrebbe aver ulteriormente favorito la diffusione dell’infezione. L'applicazione delle misure di controllo è risultata complessa a causa della pratica diffusa del pascolo promiscuo, dell’assenza di indennizzi statali per gli abbattimenti e della conseguente scarsa collaborazione degli allevatori. Il rapporto della missione European Union Veterinary Emergency Team (EUVET) raccomanda il potenziamento della sorveglianza sierologica negli ovini, l'avvio rapido di una strategia vaccinale e l'invio di campioni al laboratorio di riferimento dell’Unione Europea (presso il “Centre de coopération internationale en recherche agronomique pour le développement”, Montpellier, Francia) per la caratterizzazione genetica del ceppo circolante, al fine di chiarire l’origine dell'introduzione.
Kosovo (2025): a causa dell’estensione della diffusione della malattia in Albania, le autorità veterinarie kosovare intensificano la sorveglianza attiva, in particolare lungo la zona di confine. A luglio 2025 viene confermato il primo ed unico focolaio di PPR in un allevamento misto nella regione di Prizren, a circa 15 km dal confine albanese, con ripercussioni su un patrimonio di 178 caprini e 13 ovini. L’introduzione del virus è verosimilmente attribuita a movimenti illegali di piccoli ruminanti dall’Albania. Viene istituita una zona di protezione di 3 km; inoltre, EUVET raccomanda l’istituzione di una zona di sorveglianza di 10km, sulla base della normativa europea e la prioritizzazione dei controlli clinici e sierologici, soprattutto sui capi che rientrano dai pascoli al confine con l’Albania. L’episodio sottolinea l’importanza di una sorveglianza rafforzata e di una stretta cooperazione transfrontaliera per prevenire l’introduzione del virus in aree precedentemente indenni.
Croazia (2025): a dicembre viene confermata la prima introduzione del virus in un allevamento ovino nel comune di Prgomet, nella contea di Spalato-Dalmazia, nella parte centro-meridionale del Paese. L’infezione viene individuata nell’ambito di indagini diagnostiche differenziali avviate a seguito della comparsa di sintomatologia abortiva. Il focolaio iniziale coinvolge 26 ovini, risultati tutti sieropositivi. Le autorità dispongono l’abbattimento immediato degli animali e l’istituzione di zone di restrizione, inizialmente di 3 e 10 km, successivamente estese a 5 e 20 km. Tra dicembre 2025 e gennaio 2026 vengono notificati altri 4 focolai, tutti epidemiologicamente collegati al primo, verosimilmente per contatto diretto tra animali o pascolo promiscuo. Tra questi si segnalano anche un caso in un allevamento misto di ovini e caprini nella contea di Zara. Le autorità croate applicano rigorose misure di controllo, tra cui abbattimento, pulizia e disinfezione e visite veterinarie sistematiche nelle zone intereassate, e rafforzano i requisiti di biosicurezza su tutto il territorio nazionale. La fonte dell’infezione non viene identificata con certezza. Tuttavia, emergono criticità legate a movimenti illeciti di animali e a carenze documentali lungo il confine con la Bosnia-Erzegovina, considerati il meccanismo più probabile di introduzione. La localizzazione geografica dei focolai indica inoltre la presenza del virus sulla sponda orientale dell’Adriatico.
Nel complesso, questa sequenza di eventi non rappresenta una serie di introduzioni indipendenti, ma piuttosto il segnale di una trasmissione sostenuta tra Paesi contigui. Anche i focolai apparentemente più circoscritti, come quelli ungheresi o croati, assumono pertanto un significato epidemiologicamente rilevante, indicando che il virus circola nella regione e continua a trovare vie di diffusione attraverso le reti di movimentazione animale, sia formali sia informali.
Le analisi genetiche indicano che i ceppi virali responsabili dei focolai europei di PPR sono geneticamente correlati a quelli circolanti in Nord Africa, mentre è stata esclusa una correlazione con i ceppi presenti nella vicina Turchia. Le modalità precise di introduzione del virus rimangono tuttora oggetto di indagine, sebbene le rotte della movimentazione animale, comprese quelle informali o non tracciate, rappresentino il principale fattore di rischio per la diffusione dell’infezione in popolazioni suscettibili16.
Va inoltre considerato che numerosi focolai sono stati identificati grazie alle attività di tracciamento epidemiologico e ai test diagnostici effettuati nelle zone di restrizione. Infatti, il decorso clinico lieve della malattia può renderne difficile l’individuazione precoce.
Fonte dati: WAHIS, aggiornamento al 09/02/20269
| Data di inizio evento | Paese colpito | Focolai confermati | Casi | Morti | Data di chiusura | Sospetta fonte |
| 08/07/2024 | Grecia | 86 | 5317 | 606 | 01/01/2025 | Sconosciuta, o inconclusiva |
| 15/07/2024 | Romania (prima comparsa) | 67 | 226162 | 13761 | 02/12/2024 | Sconosciuta, o inconclusiva |
| 25/11/2024 | Bulgaria | 1 | 25 | 4 | In corso | Sconosciuta, o inconclusiva |
| 23/01/2025 | Ungheria | 3 | 433 | 30 | 31/01/2025 | Movimentazioni legali di animali |
| 03/03/2025 | Romania (ricorrenza) | 1 | 664 | 12 | 11/04/2025 | Sconosciuta, o inconclusiva |
| 03/06/2025 | Albania (prima comparsa in area circoscritta) | 10 | 271 | 67 | In corso | Sconosciuta, o inconclusiva |
| 04/06/2025 | Albania (prima comparsa nel Paese) | 3 | 179 | 86 | In corso | Sconosciuta, o inconclusiva |
| 03/07/2025 | Kosovo | 1 | 50 | 6 | *Non disponibile | Movimentazioni animali |
| 06/12/2025 | Croazia | 5 | 26 | 0 | In corso | Sconosciuta, o inconclusiva |
*Data di chiusura non disponibile. Paese non riconosciuto come stato indipendente da 5 membri UE.
Fonte dati: PAFF Committee
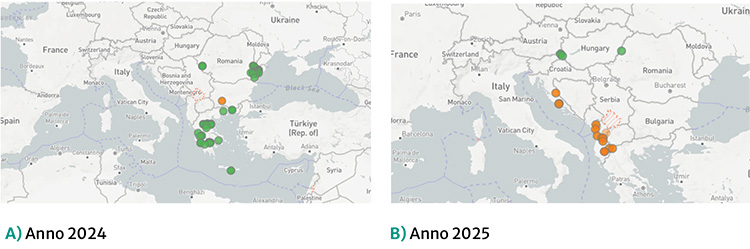 Figura 1.Distribuzione spaziale dei focolai nel Sud-Est Europa nel 2024 (A) e 2025 (B)
Figura 1.Distribuzione spaziale dei focolai nel Sud-Est Europa nel 2024 (A) e 2025 (B)
Fonte dati: WAHIS. In verde i focolai estinti, in arancione gli attivi
Dinamiche di diffusione: il contributo dell’epidemiologia molecolare
Comprendere le rotte di diffusione del virus è essenziale per indagare le possibili fonti di introduzione. In questo contesto, l'epidemiologia molecolare si è affermata come uno strumento fondamentale, in grado di trasformare singoli eventi isolati in un quadro coerente di trasmissione e di fornire informazioni di immediata utilità operativa in termini di prevenzione e controllo della malattia.
Gli studi di filogenesi condotti sui ceppi virali responsabili delle recenti incursioni indicano un’origine comune e una stretta correlazione filogenetica tra i virus isolati in Grecia, Romania e Bulgaria. In particolare, i ceppi europei appartengono al Lineage IV e mostrano una forte correlazione genetica con i ceppi circolanti in Nord Africa (Box 1)17.
| Perché i genomi sono utili anche nella gestione della malattia sul territorio? |
| Genomi tra loro molto simili in focolai distinti suggeriscono un collegamento epidemiologico o una fonte comune; differenze marcate indicano invece possibili introduzioni multiple. In termini operativi, tali informazioni contribuiscono a orientare la priorità tra azioni focalizzate sul contenimento locale e azioni mirate al rafforzamento dei controlli su ingressi e movimentazioni. |
Box 1. Interpretazione della genomica
Con una probabilità stimata tra il 97 e il 99%, la Romania è il primo Paese interessato dall’infezione16. L’analisi genomica dei focolai evidenzia la presenza di molteplici introduzioni indipendenti del virus in Europa, come indicato dall’identificazione di diversi cluster genetici derivati da un comune ceppo ancestrale. Inoltre, alcuni di questi cluster includono sequenze provenienti sia dalla Romania sia dalla Grecia, suggerendo l’esistenza di successive catene di trasmissione a livello regionale tra Paesi diversi, probabilmente favorite dai movimenti e dal commercio di animali infetti. Nell’interpretazione dell’analisi genomica vanno considerati alcuni aspetti, tra cui la mancanza di uniformità geografica nella disponibilità di sequenze provenienti dai focolai, la presenza di dati parziali derivanti da alcune indagini epidemiologiche e il fatto che in alcuni casi i campioni siano stati ottenuti diverse settimane dopo l’inizio del focolaio16.
Rivelando una quasi identità tra ceppi di focolai in Paesi diversi, l’analisi genomica rappresenta un tangibile strumento di supporto per le autorità sanitarie, consentendo di concentrare le indagini epidemiologiche sui contatti diretti e sui moviemnti di animali tra aree di interesse specifico, evitando di disperdere risorse in controlli generalizzati. Al contrario, ceppi geneticamente distinti indicherebbero vie di introduzione separate, spostando l'attenzione verso i punti di ingresso e il commercio internazionale.
Prioritizzare interventi mirati e proporzionati permette dunque di massimizzare l'efficacia della risposta e ottimizzare l'utilizzo delle risorse.
Dalla prevenzione al controllo: il dispositivo europeo contro la PPR
In vista del reale rischio di introduzione della malattia, le azioni orientate a ridurre le opportunità di incursione comprendono il rafforzamento dei controlli alle frontiere, la gestione prudente delle introduzioni di animali, la separazione dei nuovi arrivi e l’adozione di procedure essenziali di biosicurezza per limitare i contatti indiretti con mezzi, persone e attrezzature potenzialmente contaminati1.
Parallelamente, un impianto efficace di sorveglianza per PPR si basa sull’integrazione tra sorveglianza passiva e attiva. La sorveglianza passiva è basata sulla rilevazione tempestiva dei segni clinici, mentre la sorveglianza attiva viene condotta in contesti identificati come a rischio, quali aree ad alta movimentazione, mercati e territori adiacenti a zone interessate da focolai.
Indipendentemente dal tipo di sorveglianza svolta, in presenza di un sospetto, la Real-Time RT-PCR rappresenta il gold standard per la conferma diagnostica, in grado di fornire un risultato in poche ore. Per casi confermati, deve seguire la caratterizzazione genomica, che alimenta il sistema di intelligence dell'epidemiologia molecolare. La sinergia tra un sistema di sorveglianza sensibile e una rete diagnostica rapida e precisa costituisce l'infrastruttura per una gestione efficace dell'emergenza.
Essendo la PPR una malattia di categoria A, in attesa della conferma è necessaria una risposta precoce e conservativa che, nel quadro del Regolamento (UE) 2016/429 e Regolamento Delegato 2020/687, prevede in Europa, il blocco delle movimentazioni, il tracciamento, l’istituzione di zone di protezione e sorveglianza e isolamento degli animali sospetti infetti (Box 2).
| Separare il capo o capi con sintomatologia sospetta |
| Blocco delle movimentazioni |
| Attivazione delle autorità veterinarie e del sistema diagnostico |
| Rintraccio dei movimenti degli animali |
Box 2. Azioni previste in caso di sospetto
In caso di conferma, lo stesso regolamento prevede misure stringenti sul focolaio, finalizzate all’eradicazione della malattia, illustrate nel Box 3.
| Sequestro dell’allevamento con blocco immediato di tutte le movimentazioni e avvio dell’indagine epidemiologica |
| Notifica immediata dell’evento alla Commissione Europea tramite l’Animal Diseases Information System (ADIS), integrato con il sistema di notifica internazionale WAHIS del WOAH18 |
| Abbattimento di tutti gli animali suscettibili presenti nell’unità epidemiologica, gestione e smaltimento in sicurezza di carcasse e materiali contaminati, seguiti da pulizia e disinfezione di tutti i locali, attrezzature e mezzi sotto supervisione ufficiale |
| Istituzione delle zone di protezione (raggio di 3 km) e di sorveglianza (raggio di 10 km) attorno al focolaio, all’interno delle quali viene attivata una sorveglianza veterinatia intensificata |
Box 3. Azioni previste in caso di conferma
Implicazioni per l’Italia e risposta dell’Italia al rischio PPR
In questo contesto di crescente pressione infettiva, lo status di indennità dell'Italia rappresenta una condizione da preservare mediante azioni consapevoli e proattive.
Se da una parte l'assenza di notifiche nel sistema europeo WAHIS conferma l’indennità attuale, dall’altra evidenzia la vulnerabilità del Paese. La posizione geografica della penisola, infatti, protetta solo in parte dalle barriere naturali, la espone a un rischio di spillover multifattoriale. La prossimità con i nuovi focolai balcanici, in particolare quelli croati, costituisce una minaccia diretta e immediata. Il commercio transadriatico, sia legale sia illegale, rappresenta un potenziale canale di introduzione silente. A questo si aggiunge la rilevante densità di allevamenti ovicaprini in alcune regioni del Nord-Est d’Europa, che, una volta introdotto il virus, ne favorisce una diffusione rapida ed estesa. La combinazione di questi fattori – vicinanza geografica, intensità di scambi e suscettibilità della popolazione animale – giustifica la necessità di mantenere elevata l’attenzione soprattutto in termini di capacità di riconoscimento precoce del sospetto clinico, rapidità di attivazione del canale diagnostico, applicazione tempestiva delle misure di controllo e gestione della comunicazione lungo tutta la filiera. Questo si traduce nel mantenere un elevato livello di allerta tra tutti gli attori della filiera: dagli allevatori, ai veterinari libero-professionisti, fino agli Istituti Zooprofilattici Sperimentali (IIZZSS).
Per questo motivo, l'Italia ha attivato un sistema di sorveglianza straordinaria volto a prevenire l'introduzione del virus sul territorio nazionale. Il Ministero della Salute, tramite la Direzione Generale della Sanità Animale (DGSAF), ha emanato nel luglio 2024 una circolare operativa che ha innalzato il livello di attenzione su tutte le importazioni di ovi-caprini provenienti da aree epidemiologicamente interessate, raccomandando controlli mirati19. Il sistema si articola su più livelli, coinvolgendo diverse componenti della rete veterinaria pubblica. In prima istanza, gli Uffici Veterinari per gli Adempimenti Comunitari (UVAC), strutture periferiche del Ministero della Salute preposte alla vigilanza sugli scambi intracomunitari, hanno proceduto all'analisi dei flussi commerciali registrati nel sistema TRACES (Trade Control and Expert System - piattaforma online della Commissione Europea per la certificazione sanitaria e fitosanitaria obbligatoria negli scambi commerciali di animali, prodotti di origine animale, alimenti, mangimi, piante e prodotti vegetali), identificando le partite di ovi-caprini provenienti dai Paesi con focolai attivi. Per ciascuna spedizione è stato attivato il Servizio Veterinario dell'ASL territorialmente competente, incaricato di verificare la documentazione di accompagnamento e di sottoporre gli animali a controllo clinico, prestando particolare attenzione a sintomatologie compatibili con la PPR.
In presenza di casi sospetti, il protocollo prevede il coinvolgimento del Centro di Referenza Nazionale per le malattie esotiche degli animali (CESME), presso l'IZS dell'Abruzzo e del Molise “G. Caporale”, Teramo. Il CESME, in qualità di Laboratorio Nazionale di Riferimento, costituisce il polo di competenza scientifica per la conferma di eventuali positività. Parallelamente, per rafforzare le competenze sul campo, il Ministero e il CESME hanno organizzato iniziative formative in forma di webinar rivolte ai veterinari pubblici, con l'obiettivo di migliorare il riconoscimento precoce della malattia e la corretta gestione dei casi sospetti.
L'efficacia di questo dispositivo risiede nella sinergia tra le diverse componenti della rete, dove il Ministero svolge una funzione di coordinamento, gli UVAC e i Servizi Veterinari locali hanno un ruolo di vigilanza e intervento sul territorio, mentre gli IIZZSS e il CESME svolgono attività diagnostica specializzata. Questo sistema integrato consente all'Italia di mantenere un monitoraggio costante del rischio, garantendo la capacità di rintracciare rapidamente le partite a rischio e di attuare, se necessario, provvedimenti mirati per proteggere il patrimonio zootecnico nazionale da una malattia a forte impatto economico e sanitario.
Conclusioni
Gli sviluppi del 2024–2025 hanno rappresentato una svolta decisiva nella storia della Peste dei piccoli ruminanti in Europa, mostrando che la malattia è diventata un pericolo concreto per contesti precedentemente indenni, imponendo un cambiamento di paradigma gestionale. Il messaggio centrale è che, in un mondo iperconnesso da flussi commerciali e movimentazioni di animali, l'indennità non è uno status permanente, ma un obiettivo da preservare attraverso un investimento costante. Per l'Italia e per gli altri Paesi europei ancora indenni, la strategia deve fondarsi su un modello integrato di vigilanza proattiva, in cui sono previsti:
- Controlli e prevenzione al confine
- Sorveglianza passiva e attiva, per garantire un rilevamento precoce
- Flusso dati efficiente e rete diagnostica rapida, in grado di fornire certezze in tempi brevi
- Piani di emergenza standardizzati, per assicurare una risposta immediata, coordinata ed efficace
- L'intelligence fornita dall'epidemiologia molecolare, a supporto delle misure di controllo.
L'obiettivo finale della strategia globale di eradicazione prevista entro il 2030, rimane valido, ma, considerando gli eventi dell’ultimo biennio, il percorso si presenta più complesso. La prevenzione dell’introduzione della malattia negli stati ancora indenni e l’eradicazione dei focolai esistenti dipendono oggi dalla capacità di trasformare la conoscenza della malattia e della sua epidemiologia in scelte operative efficaci e strutturate, in termini di prevenzione e controllo.
La persistenza di focolai attivi nell’area balcanica e nel Sud-Est europeo conferma che la pressione infettiva alle porte dell’Unione rimane elevata. In questo contesto, il rischio di introduzione attraverso la movimentazione di animali, anche informale o illegale, impone di mantenere un livello di allerta elevato attraverso sistemi di sorveglianza veterinaria strutturati e capillari, soprattutto per Paesi geograficamente esposti come l’Italia.
Ringraziamenti
Si ringrazia la Dott.ssa Francesca Dall'Acqua per il contributo fornito attraverso la condivisione di materiale tecnico e per la revisione critica del manoscritto.
Bibliografia
- FAO and OIE, 2015. Global Strategy for the Control and Eradication of PPR
- Ministero della Salute (2025) Piano Nazionale per le Emergenze di Tipo Epidemico: Manuale Operativo - Peste dei Piccoli Ruminanti. Versione Rev. 2.0, Ottobre 2025. Roma: Direzione Generale della Salute Animale, Ufficio 3 - Centro Nazionale di lotta ed emergenza contro le malattie animali. In collaborazione con: Centro di Referenza Nazionale per le Malattie Esotiche degli Animali (CESME), Istituto Zooprofilattico Sperimentale dell'Abruzzo e del Molise "G. Caporale"
- European Parliamentary Research Service. "Peste des petits ruminants: A race against time for livelihoods and livestock." July 9, 2025
- Unione Europea. (2009). Regolamento (CE) n. 1069/2009 del Parlamento Europeo e del Consiglio, del 21 ottobre 2009, recante norme sanitarie relative ai sottoprodotti di origine animale e ai prodotti derivati non destinati al consumo umano e che abroga il regolamento (CE) n. 1774/2002 (regolamento sui sottoprodotti di origine animale). Gazzetta ufficiale dell'Unione Europea, L 300, 1-33
- Unione Europea. (2016). Regolamento (UE) 2016/429 del Parlamento Europeo e del Consiglio, del 9 marzo 2016, relativo alle malattie animali trasmissibili e che modifica e abroga taluni atti in materia di sanità animale (legge sulla salute animale). Gazzetta ufficiale dell'Unione Europea, L 84, 1-208
- Commissione Europea. (2020). Regolamento delegato (UE) 2020/687 della Commissione, del 17 dicembre 2019, che integra il regolamento (UE) 2016/429 del Parlamento europeo e del Consiglio per quanto riguarda le norme relative alla prevenzione e al controllo di determinate malattie elencate. Gazzetta ufficiale dell'Unione Europea, L 174, 64-139
- Padhi, A. and Ma, L. (2014). Genetic and epidemiological insights into the emergence of peste des petits ruminants virus (PPRV) across Asia and Africa. Scientific Reports, 4, p. 7040. doi:10.1038/srep07040
- European Commission, Directorate-General for Health and Food Safety. (2024-2026). Presentations of the PAFF Committee on Animal Health and Welfare
- World Organisation for Animal Health (WOAH). (2024-2025). WAHIS event management: Peste des petits ruminants in Europe
- Commissione Europea. (2024). Decisione di esecuzione (UE) 2024/2923 della Commissione, del 20 novembre 2024, che modifica la decisione di esecuzione (UE) 2024/2132 relativa ad alcune misure di emergenza provvisorie contro l'infezione da virus della peste dei piccoli ruminanti in Grecia. Gazzetta ufficiale dell'Unione Europea, L 2923
- Kirtzalidou A, Bataille A, et al. (2025). Identification of peste des petits ruminants virus, Greece, 2024. Research in Veterinary Science, 194, 105840
- Commissione Europea. (2024). Decisione di esecuzione (UE) 2024/2154 della Commissione, del 6 agosto 2024, che modifica la decisione di esecuzione (UE) 2024/2119 relativa ad alcune misure di emergenza provvisorie contro l'infezione da virus della peste dei piccoli ruminanti in Romania. Gazzetta ufficiale dell'Unione Europea, L 2154
- Iacobescu-Marițescu I, et al. (2025). Field-based characterization of peste des petits ruminants virus outbreaks in Romania, 2024-2025. Transboundary and Emerging Diseases, 72(3), 1125-1138
- Commissione Europea. (2025). Decisione di esecuzione (UE) 2025/255 della Commissione, del 31 gennaio 2025, relativa ad alcune misure di emergenza provvisorie contro l'infezione da virus della peste dei piccoli ruminanti in Ungheria. Gazzetta ufficiale dell'Unione Europea, L 255
- SIVeMP - Società Italiana Veterinari per gli Animali da Reddito e da Compagnia. (2025). Focolaio Peste dei piccoli ruminanti in Ungheria. sivemp.it, 30 gennaio
- European Union Reference Laboratory for Peste des Petits Ruminants (EURL-PPR). (2025, August). Update on PPR emergence in Europe: Insights from viral genetic investigations [Conference presentation]. 1st GF-TADs Regional Conference in the European Region, Belgrade, Serbia. CIRAD
- Guendouz S, Bataille A, et al. (2025). Genomic analysis of peste des petits ruminants virus emergence in Greece, Romania and Bulgaria, 2024. Infection, Genetics and Evolution, 118, 105712
- European Parliamentary Research Service (EPRS). (2025). Peste des petits ruminants: The EU's response to outbreaks in South-East Europe (Briefing PE 775.865). European Parliament
- Ministero della Salute, Direzione Generale della Sanità Animale e dei Farmaci Veterinari (DGSAF). (2024). Notifica focolai di Peste dei piccoli ruminanti (PPR) in Grecia e Romania. Nota del Direttore Generale Giovanni Filippini, 24 luglio 2024.
Selene Corsini
Centro Operativo Veterinario per l’Epidemiologia, Programmazione, Informazione e Analisi del Rischio (COVEPI), Istituto Zooprofilattico Sperimentale dell’Abruzzo e del Molise “G. Caporale”, Teramo